脓毒性心肌病的VAV-ECMO治疗:单中心经验
第二十八期
2
脓毒性心肌病的VAV-ECMO治疗:单中心经验
Veno-arterio-venous ECMO for septic cardiomyopathy: a single-centre experience
Vogel DJ, et al.
Perfusion. 2018 May;33(1_suppl):57-64. doi: 10.1177/0267659118766833..
文献回顾
研究背景
脓毒性休克患者应用ECMO效果尚不清楚。VV-ECMO主要用于肺功能衰竭患者,而VA-ECMO主要用于心功能衰竭患者。对于心肺功能联合衰竭的患者来说,临床尝试应用VAV-ECMO来进行辅助支持。目前来说,VAV-ECMO多见于患者心功能恢复过程中又合并出现肺功能衰竭。但对于部分重症肺部感染患者来说,继发出现脓毒性心肌病,这类患者需要进行VAV-ECMO辅助支持。
研究目的
本研究针对VAV-ECMO辅助脓毒性心肌病成人患者的相关临床资料进行回顾性分析。
研究方法
回顾性分析成人重症呼吸衰竭合并脓毒性心肌病患者的VAV-ECMO资料。临床数据从电子病历中提取,包括一个专门的ECMO转诊和后续数据库。
研究结果
2014年1月01日至2017年12月20日,共计324例VV-ECMO病例,其中包括19(5.9%)例VAV-ECMO用于支持合并心力衰竭患者。根据临床数据对这19例患者进行分析后,排除7个病人(二尖瓣血栓形成n=1,羊水栓塞n=1,心源性休克后心肌梗死 n=1,药物过量n=2,心脏术后n=2)。参考和结果预测分数的基线数据如表1所示。评分预测和结果比较,表1中的SOFA、APACHE II和SAVE 评分预测存活率分别为:50% (初始SOFA评分中位数10),50-55% (APACHE II评分中位数 23.5)和30% (SAVE评分中位数-5.5)。
4名患者(33.3%) 最初是VV-ECMO随后在转至我院后置入动脉插管转为VAV-ECMO。8名患者为VAV-ECMO,其中一个最初为VV-ECMO支持,但在转运之前的观察期内即转换为VAV-ECMO。5个病人(41.7%)在启动ECMO支持前发生心脏骤停,经历CPR过程。
插管方式为:静脉引流:左股静脉,25Fr多级股静脉插管;静脉回流:右颈静脉,23Fr静脉插管;动脉回流:右股动脉,17Fr动脉插管。另外经超声引导下Seldinger法在股总动脉置入7或8 Fr增强回流管逆行灌注动脉插管侧下肢
。
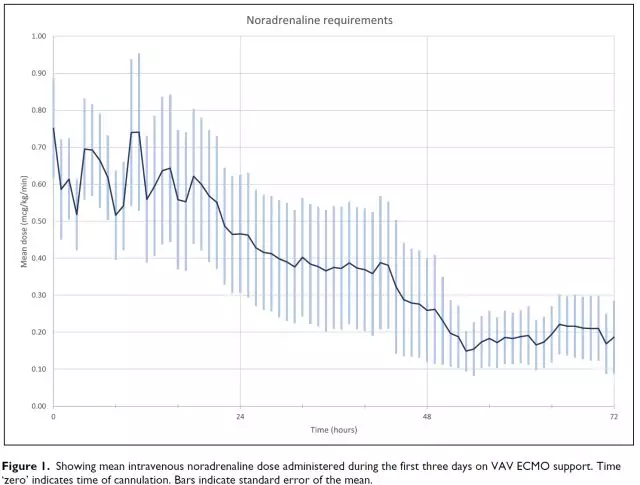
所有患者均接受去甲肾上腺素,每小时用量如图1所示。此外,每个病人以0.10μg/kg/h的速率连续注射左西孟旦。
图2血乳酸的变化:ECMO启动前6h内最差值以及转流开始之后的每6h中最差值。
在心脏支持和监测方面,所有病人均监测LVEF值,12例患者基线经胸超声心动图均显示严重的左心功能损伤。上机时左室射血分数(LVEF)中位数为16.25% (IQR 13.13 -17.5)。其中8例患者还显示右心功能损害。
主动脉瓣上血流时间速度积分(AV VTI)作为常规撤机评估项目,在撤除动脉插管前平均AV VTI为17.7 cm (IQR 16.7-19),在动脉流量≤1 L/min时LVEF中位数为41.25% (IQR 34.38-43.75)。
存活患者LVEF值均恢复正常(LVEF:55-60%),首次记录到正常EF的中位时间为9天(IQR 4-12天),3例死亡患者LVEF值也较辅助之前有所提高(最后一次LVEF分别为40,40和50%),1例患者行冠脉造影检查(排除冠心病),并在VAV-ECMO运行后因超声示左心膨胀而加装IABP左心减压,IABP运行5天。其余患者无机械辅助支持以及左心减压和其他诊断性或治疗性的心脏干预。
1例患者撤机后行心内膜下心肌活检,本例中心肌细胞未发现肥大,杂乱,明显的炎性反应,纤维化,肉芽肿或铁沉积,刚果红淀粉样蛋白染色呈阴性。
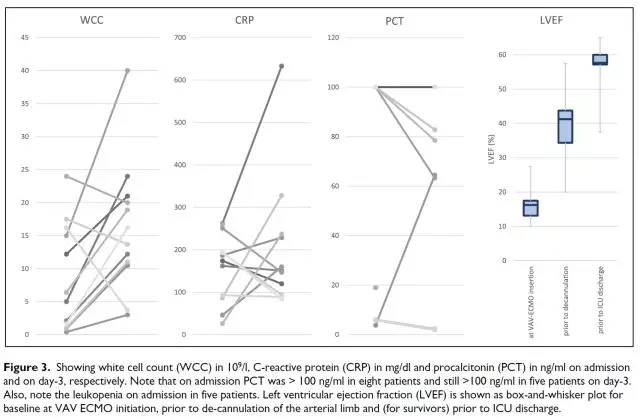
病原体的检查发现,在11个病例中(91.7%)发现明确病原体。75%确诊为革兰氏阳性球菌感染。炎症标记物如图3所示。
根据我们当地指南,脓毒性休克患者的治疗方案为针对核糖体蛋白质合成的联合抗生素治疗。在ECMO启动后48小时内,6/12 (50%)患者使用庆大霉素,7/12 (58.3%)使用大环内酯类,3/12 (25%)使用克林霉素和9/12 (75%)使用利奈唑胺。额外支持疗法包括10/12 (83.3%)的患者(平均2 g /kg,总剂量范围1-3g /kg) 静脉注射免疫球蛋,10/12 (83.3%)患者注入8mg/h氢化可的松,7/12 (58.3%)的病人注入高剂量Pabrinex®(维生素B1、2、3、6和C)进行免疫调节/毒素清除。
并发症方面,1例患者因肢体远端置管时血管过度收缩而置管失败,发生动脉插管侧肢体远端缺血,后死于脑疝;另1例患者因发生DIC而输注红细胞。2例患者发生缺血性卒中导致的神经系统损害,1例留有右侧后遗症另1例则完全恢复。另有1例发生双侧下肢缺血和脾梗死,最终双下肢截肢。
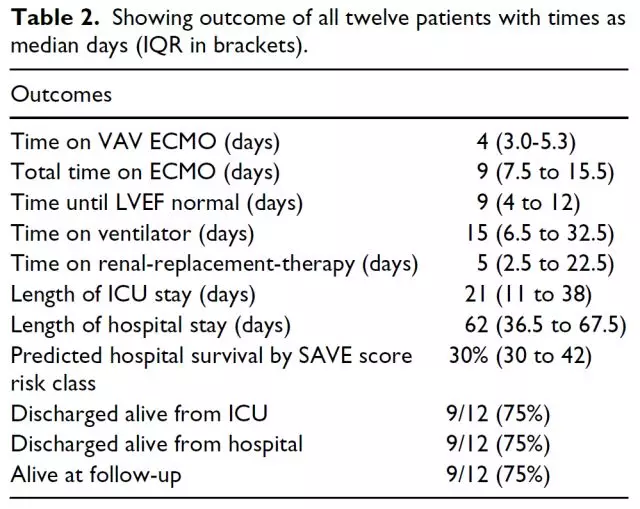
结果见表2,12例患者ECMO平均辅助时间96 h(IQR 71.25-126)中3例患者死亡,9例存活,随访6个月。
研究讨论
本研究中,VAV-ECMO治疗脓毒性心肌病的存活率结果优于现有的评分系统预测值。本结果和Bréchot等报道的使用VA-ECMO治疗重症脓毒性心肌病的结果(14例,存活率71%)相似。相比其他报道,存活率更高。虽然各文献结果不一致,但脓毒性心肌病确是死亡的独立危险因素。本组患者心功能受损严重,且存在脏器衰竭和乳酸超高,但心脏功能平均4天恢复,心功能紊乱并非致死因素,心肌活检的结果也可以佐证这点。相对于缺血性心肌病,此类患者心功能恢复所需时间更短,而且左心膨胀的病例也很少,仅有1例放置IABP。在循环支持和全身氧供得到有效改善的情况下,脓毒性心肌病可迅速恢复。
VAV-ECMO利用“Y”形接头将动脉血分为两路,分别供应股动脉和颈静脉,根据患者的心肺功能状况以及监测右上肢血气以及脉搏氧饱和度以及脑氧饱和度来持续调整两侧的合理分流量大小,避免出现上下半身氧供不匹配。心脏功能的恢复一般早于肺的恢复,撤呼吸支持的时间平均为9天。5例患者在最初VV-ECMO启动后几小时后转为VAV-ECMO,有的是因为心功能急剧恶化,有的是留时间评估单独VV-ECMO对心功能损伤的作用。在低氧血症和高碳酸血症得到纠正后,心功能也会得到改善。右心功能得到改善后,胸内压会下降,同时左心功能也会得到改善。心功能状况不断变化且难以预测时,VAV-ECMO可以有效维持中枢的氧供。
通过肺灌洗液的检查发现,致病菌为葡萄球菌或链球菌,可引起严重感染且其释放的毒素引起白细胞升高和加剧组织坏死。机体反应为2/3的患者降钙素原超过100 ng/ml,约半数的患者白细胞显著减少,可见这2个指标既提示脓毒症的严重程度也提示产毒素微生物的存在。
2例并发症一例为侧枝灌注管置管困难,1例为出血。经超声和透视引导外周插管只安全有效的,不过最好有外科医生后备,在置管失败时可由外科置管。其他并发症还包括脑出血和脊髓梗塞。VA-ECMO本身可能导致脑的栓塞和出血事件,而VV-ECMO则可能引起颅内出血,所以ECMO病人其实很难判断并发症的出现是由ECMO引发还是有疾病本身引起。
本研究缺陷在于是小样本非对照回顾性观察,治疗模式由临床医生决定。将来的研究重点是明确VAV-ECMO治疗脓毒性心肌病的有效性。
结论
脓毒性心肌病是由于脓毒性休克内毒素释放引发的心功能受损,是可恢复的。VAV-ECMO治疗脓毒性休克尚无充足证据。我院的VAV-ECMO治疗脓毒性心肌病结果优于常规评分系统。
此类患者的治疗充满挑战,需要丰富的经验和专业知识来启动、维护ECMO及处理ECMO可能导致的并发症。在大的呼吸中心,对于脓毒性心肌病继发的脓毒性休克合并呼吸衰竭的这一部分病人,VAV-ECMO是行之有效的救治措施。将来仍需进一步开展对比不同的体外支持策略相对于传统复苏手段的研究。
本期文献回顾
刘刚 中国医学院阜外医院
编辑 | 李勇男
审校| 楼松